Resultatene fra registreringsstudiene på ankyloserende spondylitt (MEASURE 1 og 2), ikke-radiografisk aksial spondyloartritt (PREVENT), psoriasisartritt (FUTURE 1 og 2) og psoriasis (ERASURE og FIXTURE) er publisert og er bakgrunnen for myndighetenes vurdering og godkjenning. For å oppnå optimal bruk av sekukinumab og en dypere forståelse av legemidlets effekt og sikkerhetsprofil gjennomfører, Novartis og akademiske forskere verden over flere studier på sekukinumab. Det pågår også mye forskning på cytokin IL-17A og hvilken rolle det spiller for sykdom og helse. Nedenfor finner du lenker til noen artikler med studieresultater for sekukinumab og IL-17A.
Av Morten Bahrt Haulrig, Hudlege ved Gentofte Hospital i Danmark.
Psoriasis er en kronisk inflammatorisk sykdom som påvirker 2-3% av den vestlige befolkningen, likt fordelt blant menn og kvinner.1 Sykdomstidspunktet er bimodal, med topper rundt 16-22 år og 57-60 år, men omtrent en tredjedel av pasientene har allerede hatt sykdomsbegynnelse når de fyller 16 år.2,3 Samlet prevalens hos personer under 18 år er rapportert å være mellom 0-2%, med en lineær økning i forekomst fra 0,1% ved 1 år til 1,2% ved 18 år.4–6 Psoriasis er dermed ikke en sjelden sykdom i barndommen.
Typer
Psoriasis kan deles inn i forskjellige kliniske manifestasjoner. Den vanligste manifestasjonen hos både barn og voksne er psoriasis vulgaris, som forekommer hos 35-70% av barn med psoriasis.7 Guttat psoriasis forekommer hos 6-26% av barn med psoriasis, som er hyppigere enn hos voksne.8 Guttat psoriasis utløses ofte av streptokokkoltonsillitt, og omtrent en tredjedel av barn med guttat psoriasis står i fare for å utvikle plakkpsoriasis senere i livet. 9,10
Forekomsten av de andre manifestasjonene er mindre hyppig, med 3,6% for blepsoriasis, invers psoriasis 1,5%, pustuløs psoriasis 0,5-3% og neglepsoriasis 0,6%.7–9 Generelt er hodebunnen og ansiktet de mest berørte områdene etterfulgt av lyske, truncus, samt ekstensorflatene på knærne og albuene.3,5,7,8
Diagnostikk
Hos barn kan diagnosen være vanskeligere å stille på grunn av et mildere sykdomsbilde, med små, tynne plakk i forhold til hos voksne. I tillegg ses atypiske manifestasjoner, noe som kan gjøre det utfordrende å skille sykdommen fra andre hudsykdommer som atopisk dermatitt, seboreisk dermatitt og soppsykdommer12–14. Diagnostikk hindres videre av det faktum at et sett med felles validerte studiebaserte diagnostiske kriterier for psoriasis ikke er utviklet hos barn eller voksne på dette tidspunkt.15
Patogenesen
Patogenesen av psoriasis er kompleks og avhenger av et samspill mellom hud og immunsystem, samt genetiske og miljømessige faktorer. I utgangspunktet er T-cellemediert inflammatorisk sykdom preget av keratinocytt hyperproliferasjon, vaskulær endotelproliferasjon, samt inflammatorisk celleinfiltrasjon av dermis og epidermis.16 Tvillingstudier har vist at risikoen for å utvikle psoriasis skyldes genetiske faktorer i opptil 70% av tilfellene, og det er en økt forekomst av sykdommen hos barn og barnebarn av pasienter med psoriasis sammenlignet med resten av bakgrunnspopulasjonen.17,18 Konkordansraten for eneggede og toeggede tvillinger er henholdsvis åtte og fire ganger sammenlignet med bakgrunnspopulasjonen.18 Arverekken er kompleks, og mer enn 80 kromosomale loci har per nå blitt identifisert med statistisk signifikant kobling til psoriasis.19
Flere miljøfaktorer kan utløse psoriasis og forverre allerede kjent sykdom. Av viktige årsaker hos barn er psykisk stress, fysiske traumer (Köbnerfenomen) og streptocottonsillit spesielt kjent.8,10
Komorbiditeter
Psoriasis i barndommen er forbundet med opptil dobbelt så høy risiko for å utvikle komorbiditeter sammenlignet med friske individer.5 Disse komorbiditetene inkluderer somatiske lidelser som hyperlipidemi, overvekt, hypertensjon, diabetes mellitus, polycystisk eggstokksyndrom (PCOS), alkoholfri leversykdom, revmatoid artritt og Crohn’s. I tillegg er det økt risiko for å utvikle psykiske lidelser som depresjon og angst.21–23 Forekomsten av psoriasisartritt hos barn med psoriasis er lavere enn hos voksne, med prevalens på rundt 3% hos barn sammenlignet med 22% hos voksne i Europa.23 I tillegg har det blitt påvist en sammenheng mellom psoriasis hos barn og prenatal eksponering for tobakk, og derfor kan røyking under graviditet spille en rolle i utviklingen av psoriasis.24
Psoriasis har en negativ innvirkning på livskvaliteten til både barn og voksne på samme nivå som kreft, hjertesykdom og depresjon. Sykdommen er assosiert med barn med økt stigma i form av mobbing og skam. Observasjon av livskvaliteten til barn med psoriasis hindres av det faktum at det for tiden ikke er noe psoriasisspesifikk måleverktøy for livskvaliteten til barn og ungdom.25–27
Behandling
Utdanning og sykdomsutdanning av foreldre er grunnleggende for håndteringen av psoriasis. Blant annet kan det informeres om at sykdommen ikke er smittsom, ikke dødelig og at det ikke er kurativ behandling. På samme måte at det ikke er noen restriksjoner på sport, skole og vaksiner, og at barnet i de fleste tilfeller kan leve et liv på lik linje med andre barn som ikke lider av sykdommen.12
Behandling av psoriasis kan generelt deles inn i topisk behandling, fototerapi, ikke-biologisk systemisk behandling og biologisk behandling. Det er for tiden ingen orale systemiske behandlinger godkjent for barn.28 Mildere tilfeller kan behandles med topiske steroider, som tradisjonelt har blitt gjort ved psoriasis hos barn. I tillegg kan det behandles med aktuelle vitamin D analoger, enten alene eller i kombinasjon med topisk steroid. Vitamin D-analoger er godkjent for barn over 6 år, mens kombinasjonsbehandlinger er godkjent for barn over 12 år.
Disse tradisjonelle behandlingsmodalitetene for psoriasis kan forsøkes ved mild til moderat psoriasis. Imidlertid brukes de sjelden på grunn av luktplager, og det er få studier på effekten av disse behandlingene hos barn.
Fototerapi har tradisjonelt blitt brukt mot psoriasis i mange år. Smalspektret UVB (NB-UVB) regnes som den mest effektive og milde fototerapien. Fototerapi fører imidlertid generelt til økt risiko for akselerert aldring av huden, samt økt risiko for hudkreft og bør derfor vurderes fra sak til sak.29
Biologisk medisin er immunmodulerende terapi som regulerer betennelse via bestemte veier. Biologisk behandling er indikert ved moderat til alvorlig psoriasis, som ikke har respondert på tidligere topisk eller ikke-biologisk systemisk behandling. Fem biologiske legemidler til barn er for tiden godkjent av EMA. Disse er etanercept, adalimumab, ustekinumab, iksekizumab og sekukinumab. Adalimumab og etanercept er godkjent for henholdsvis barn over 4 og 6 år og arbeider ved å binde den proinflammatoriske cytokinen TNF, som spiller en viktig rolle i autoimmun betennelse. Ustekinumab er godkjent for barn over 6 år og er et humant monoklonalt antistoff som binder seg til cytokin IL-12 og IL-23 og dermed hemmer immunaktivering. Iksekizumab og sekukinumab er godkjent for psoriasis hos barn fra seks år. Begge medisinene er også monoklonale antistoffer, som virker ved å binde seg til cytokin IL-17A. Dette hemmer immunaktivering og reduserer den inflammatoriske responsen.
Det er per i dag ingen spesifikk behandlingsveiledning for valg av biologisk behandling hos barn. I henhold til de nylig publiserte tyske retningslinjene prioriteres adalimumab som biologisk førstevalg etterfulgt av etanercept eller ustekinumab.28 Det skal imidlertid bemerkes at denne publikasjonen ble publisert før iksekizumab og sekukinumab ble godkjent for behandling av psoriasis hos barn.
Det er ingen tegn på kumulativ toksisitet eller interaksjoner med andre medisiner som bruker biologisk medisin, og derfor kan dette brukes til langsiktig behandling. Studier på langtidsdata hos voksne er tilgjengelige for de fleste biologiske behandlinger. Den immundempende effekten fører imidlertid til økt risiko for infeksjon og er betydelig dyrere enn tradisjonell ikke-biologisk behandling og eldre biologiske behandlinger. Behandling med biologisk behandling bør derfor vurderes nøye i det enkelte tilfellet.
Flere legemidler til behandling av psoriasis testes fortsatt hos barn. Dette må betraktes som en positiv utvikling som på lang sikt kan føre til et bredere spekter av effektive behandlinger.
Referanser
-
Christophers E. Psoriasis - Epidemiology and clinical spectrum. Clin Exp Dermatol. 2001;26(4):314-320. doi:10.1046/j.1365-2230.2001.00832.x
-
Henseler T, Christophers E. Psoriasis of early and late onset: Characterization of two types of psoriasis vulgaris. J Am Acad Dermatol. 1985;13(3):450-456. doi:10.1016/S0190-9622(85)70188-0
-
Raychaudhuri SP, Gross J. A comparative study of pediatric onset psoriasis with adult onset psoriasis. Pediatr Dermatol. 2000;17(3):174-178. doi:10.1046/j.1525-1470.2000.01746.x
-
Michalek IM, Loring B, John SM. A systematic review of worldwide epidemiology of psoriasis. J Eur Acad Dermatology Venereol. 2017;31(2):205-212. doi:10.1111/jdv.13854
-
Augustin M, Glaeske G, Radtke MA, Christophers E, Reich K, Schäfer I. Epidemiology and comorbidity of psoriasis in children. Br J Dermatol. 2010;162(3):633-636. doi:10.1111/j.1365-2133.2009.09593.x
-
Fotiadou C. AHMT-36672-management-of-psoriasis-in-adolescence. Published online 2014:25-34.
-
Morris A, Rogers M, Fischer G, Williams K. Childhood psoriasis: A clinical review of 1262 cases. Pediatr Dermatol. 2001;18(3):188-198. doi:10.1046/j.1525-1470.2001.018003188.x
-
Blegvad C, Nybo Andersen A-M, Groot J, Zachariae C, Barker J, Skov L. Clinical characteristics including cardiovascular and metabolic risk factors in adolescents with psoriasis. J Eur Acad Dermatol Venereol. 2020;34(7):1516-1523. doi:10.1111/jdv.16229
-
Lysell J, Tessma M, Nikamo P, Wahlgren C-F, Ståhle M. Clinical characterisation at onset of childhood psoriasis - a cross sectional study in Sweden. Acta Derm Venereol. 2015;95(4):457-461. doi:10.2340/00015555-1986
-
Boehncke WH, Schön MP. Psoriasis. Lancet. 2015;386(9997):983-994. doi:10.1016/S0140-6736(14)61909-7
-
Martin BA, Chalmers RJ, Telfer NR. How great is the risk of further psoriasis following a single episode of acute guttate psoriasis? Arch Dermatol. 1996;132(6):717-718. doi:10.1001/archderm.1996.03890300147032
-
Mahé E. Childhood psoriasis. Eur J Dermatology. 2016;26(6):537-548. doi:10.1684/ejd.2016.2932
-
Griffiths CE, Barker JN. Pathogenesis and clinical features of psoriasis. Lancet. 2007;370(9583):263-271. doi:10.1016/S0140-6736(07)61128-3
-
Kouwenhoven TA, Bronckers IMGJ, van de Kerkhof PCM, Kamsteeg M, Seyger MMB. Psoriasis dermatitis: an overlap condition of psoriasis and atopic dermatitis in children. J Eur Acad Dermatology Venereol. 2019;33(2):e74-e76. doi:10.1111/jdv.15213
-
Burden-Teh E, Phillips RC, Thomas KS, Ratib S, Grindlay D, Murphy R. A systematic review of diagnostic criteria for psoriasis in adults and children: evidence from studies with a primary aim to develop or validate diagnostic criteria. Br J Dermatol. 2018;178(5):1035-1043. doi:10.1111/bjd.16104
-
Nestle FO, Kaplan DH, Barker J. Psoriasis. N Engl J Med. 2009;361(5):496-509. doi:10.1056/NEJMra0804595
-
Farber EM, Nall ML. The natural history of psoriasis in 5,600 patients. Dermatologica. 1974;148(1):1-18. doi:10.1159/000251595
-
Lønnberg AS, Skov L, Skytthe A, Kyvik KO, Pedersen OB, Thomsen SF. Heritability of psoriasis in a large twin sample. Br J Dermatol. 2013;169(2):412-416. doi:10.1111/bjd.12375
-
Strange A, Capon F, Spencer CCA, et al. A genome-wide association study identifies new psoriasis susceptibility loci and an interaction between HLA-C and ERAP1. Nat Genet. 2010;42(11):985-990. doi:10.1038/ng.694
-
Takeshita J, Grewal S, Langan SM, et al. Psoriasis and comorbid diseases: Epidemiology. J Am Acad Dermatol. 2017;76(3):377-390. doi:10.1016/j.jaad.2016.07.064
-
Kimball AB, Wu EQ, Guérin A, et al. Risks of developing psychiatric disorders in pediatric patients with psoriasis. J Am Acad Dermatol. 2012;67(4):651-657.e2. doi:10.1016/j.jaad.2011.11.948
-
Tollefson MM, Van Houten HK, Asante D, Yao X, Kremers HM. Association of psoriasis with comorbidity development in children with psoriasis. JAMA Dermatology. 2018;154(3):286-292. doi:10.1001/jamadermatol.2017.5417
-
Alinaghi F, Calov M, Kristensen LE, et al. Prevalence of psoriatic arthritis in patients with psoriasis: A systematic review and meta-analysis of observational and clinical studies. J Am Acad Dermatol. 2019;80(1):251-265.e19. doi:10.1016/j.jaad.2018.06.027
-
Groot J, Nybo Andersen AM, Blegvad C, Pinot de Moira A, Skov L. Prenatal, infantile, and childhood tobacco exposure and risk of pediatric psoriasis in the Danish National Birth Cohort offspring. J Am Acad Dermatol. Published online 2020:1-8. doi:10.1016/j.jaad.2019.09.038
-
Randa H, Todberg T, Skov L, Larsen LS, Zachariae R. Health-related quality of life in children and adolescents with psoriasis: A systematic review and meta-analysis. Acta Derm Venereol. 2017;97(5):555-563. doi:10.2340/00015555-2600
-
Rapp SR, Feldman SR, Exum ML, Fleischer AB, Reboussin DM. Psoriasis causes as much disability as other major medical diseases. J Am Acad Dermatol. 1999;41(3):401-407. doi:10.1016/S0190-9622(99)70112-X
-
de Jager MEA, De Jong EMGJ, Evers AWM, Van De Kerkhof PCM, Seyger MMB. The burden of childhood psoriasis. Pediatr Dermatol. 2011;28(6):736-737. doi:10.1111/j.1525-1470.2011.01489.x
-
Eisert L, Augustin M, Bach S, et al. S2k guidelines for the treatment of psoriasis in children and adolescents - Short version part 2. J Dtsch Dermatol Ges. 2019;17(8):856-870. doi:10.1111/ddg.13907
-
Eisert L, Augustin M, Bach S, et al. S2k guidelines for the treatment of psoriasis in children and adolescents – Short version part 1. J der Dtsch Dermatologischen Gesellschaft. 17(8):856-870. doi:10.1111/ddg.13907
MAXIMISE - er den første randomiserte kliniske studien som viser effekten av et biologisk legemiddel i en pasientgruppe som lever med psoriasisartritt med aksial involvering
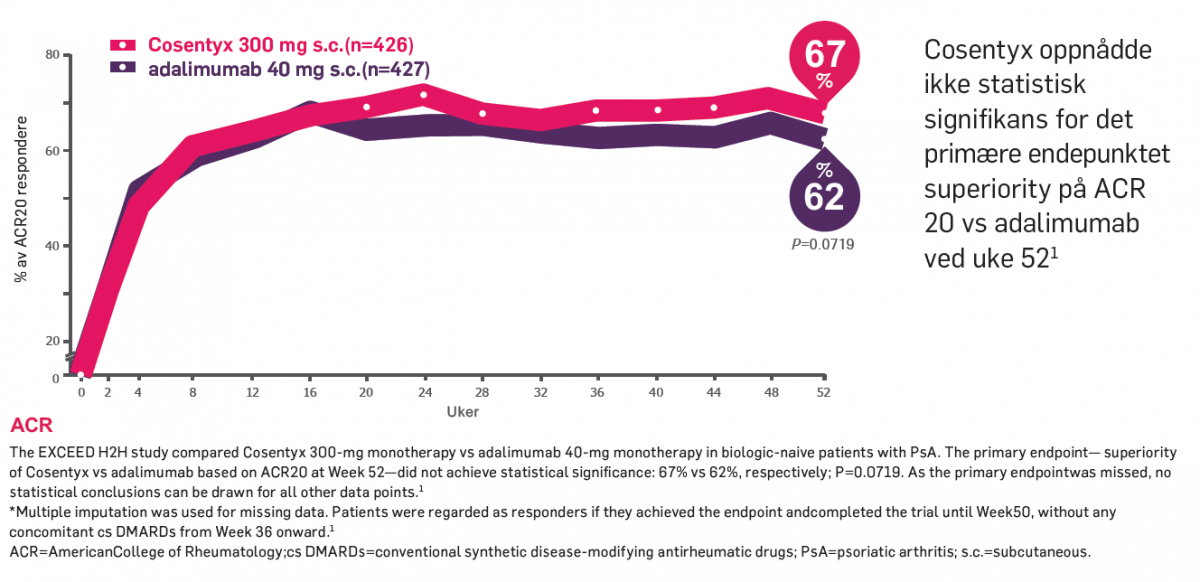
EXCEED - Direkte sammenlignende studie mellom sekukinumab og adalimumab ved PsA
Cosentyx oppnådde ikke statistisk signifikans for det primære endepunktet superiority på ACR 20 vs. adalimumab ved uke 52, men viste samtidig effektiv symptomlindring på leddplager med Cosentyx 300 mg hos biologisk naive pasienter gjennom 52 uker.
Primære resultater fra de pivotale studiene (FUTURE 1 og 2) ved bruk av sekukinumab mot PsA
Stor studie på PsA - 996 pasienter
FUTURE 5-studien med Cosentyx er den største studien som har vært gjort med et biologisk legemiddel mot PsA noen gang, med hele 996 pasienter inkludert. Resultatene viser god effekt på primære og sekundære endepunkter og en sikkerhetsprofil i tråd med det som er vist i tidligere Cosentyx-studier.
Resultater fra studier med lengre varighet enn 1 år
Tre års effekt- og sikkerhetsdata fra den pivotale FUTURE 1-studien med Cosentyx mot psoriasisartritt. Resultatene viste at effekten var opprettholdt over tid og med liten radiografisk progresjon. Sikkerhetsdatene viste at Cosentyx var godt tolerert med en sikkerhetsprofil i tråd med tidligere publikasjoner.
5 års oppfølging av PsA-pasienter fra FUTURE 1-studien. Viser god effekt over tid og med ingen nye sikkerhetssignaler. Pasienter som titrerte opp fra 150 mg til 300 mg opplevde bedre effekt.
Sekukinumab som behandling etter TNFα-hemmer ved PsA
Effekten av sekukinumab på utviklingen av strukturelle skader ved PsA
Effekten av sekukinumab på PsA i studier på moderat til alvorlig plakkpsoriasis
Sammenfattende artikkel om IL-17A og patogenesen til PsA samt resultater fra kliniske studier på sekukinumab
Andre publikasjoner
Resultater fra direkte sammenlignende studier (FIXTURE og CLEAR) ved bruk av secukinumab ved moderat til alvorlig plakkpsoriasis
Sammenstilte sikkerhetsanalyser
En stor sikkerhetsanalyse basert på 21 forskjellige studier på Cosentyx og 7355 pasienter fra de godkjente indikasjonene psoriasis, psoriasisartritt og ankyloserende spondylitt, viser at forekomsten av inflammatorisk tarmsykdom (Crohns sykdom, ulcerøs kolitt og uspesifisert IBD) er lav.
Utvikling av legemiddelantistoffer (immunogenitet)
Oversiktsartikler om IL-17
PREVENT-studien er bakgrunnen for den nye indikasjonen nr-axSpA. Preventstudien viser at sekukinumab har en rask innsettende og vedvarende effekt ved nr-axSpA. De primære endepunktene var ved uke 16 og med vedvarende effekt til uke 52.
Sikkerhetsprofilen er lik som for de andre indikasjonene og i tråd med tidligere publikasjoner.
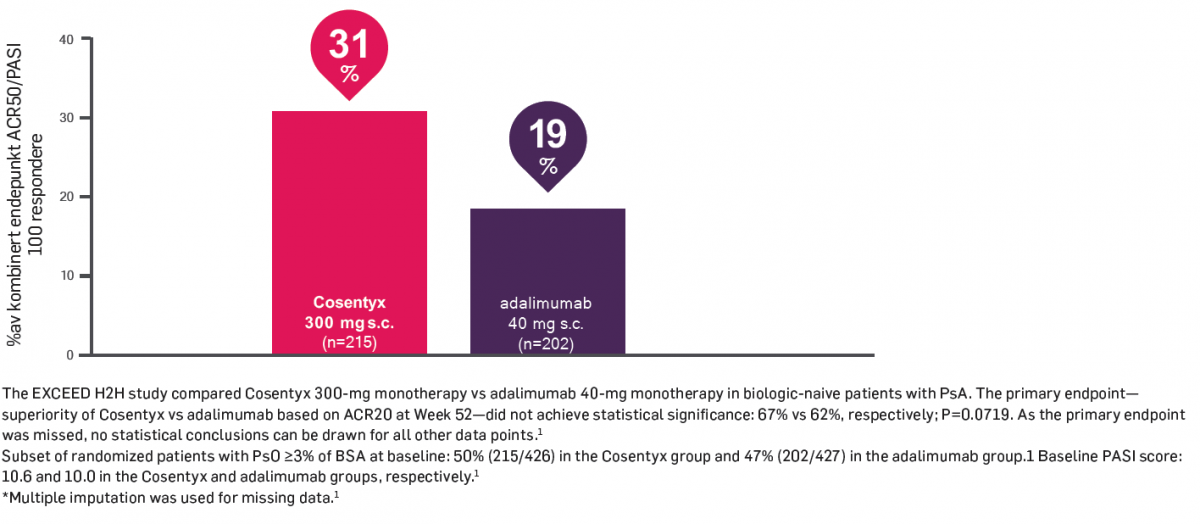
En effektiv symtomlindring på leddplager med Cosentyx 300mg hos biologisk naive pasienter gjennom 52 uker1
Over 30% av biologisk naive pasienter oppnådde det kombinerte endepunktet ACR50 og PASI100 med Cosentyx ved uke 521
Referanser
Sikkerhet og effekt av sekukinumab ble vurdert i fire randomiserte, dobbeltblinde, placebokontrollerte fase III-studier hos pasienter med moderat til alvorlig plakkpsoriasis, som var aktuelle for fototerapi eller systemisk behandling [ERASURE, FIXTURE, FEATURE, JUNCTURE]. Effekt og sikkerhet av 150 mg og 300 mg sekukinumab ble undersøkt i forhold til enten placebo eller etanercept. I tillegg vurderte en studie et kronisk behandlingsregime i forhold til et “behandling ved behov”-regime [SCULPTURE]. (SPC kap 5.1 28.04.2020)
Les mer om ERASURE og FIXTURE
- Langley RG et al. Secukinumab in plaque psoriasis--results of two phase 3 trials [ERASURE and FIXTURE]. N Engl J Med. 2014 Jul 24;371(4):326-38
Les mer om FEATURE
Les mer om JUNCTURE
Les mer om SCULPTURE
I en ytterligere psoriasisstudie (CLEAR) ble sekukinumab sammenlignet med ustekinumab (SPC kap 5.1 20-JAN-2022)
Les mer om CLEAR
- Thaçi D, Blauvelt A, Reich K et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate to severe plaque psoriasis: CLEAR, a randomized controlled trial. J Am Acad Dermatol. 2015 Sep;73(3):400-9.
- Blauvelt A, Reich K, Tsai TF et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate-to-severe plaque psoriasis up to 1 year: Results from the CLEAR study. J Am Acad Dermatol. 2017 Jan;76(1):60-69.e9.
Sekukinumab er også studert hos pasienter med spesifikke lokasjoner/undergrupper av plakkpsoriasis. I to placebokontrollerte studier ble det sett forbedring både ved neglepsoriasis (TRANSFIGURE, 198 pasienter) og palmoplantar plakkpsoriasis (GESTURE, 205 pasienter). En ytterligere placebokontrollert studie undersøkte 102 pasienter med moderat til alvorlig hodebunnspsoriasis, definert ved at man har en "Psoriasis Scalp Severity Index" (PSSI) score på ≥12, en IGA mod 2011 kun hodebunn score på 3 eller høyere og minst 30 % av hodebunnen påvirket.
Les mer om bruk av sekukinumab i ulike manifestasjoner av psoriasis
Les mer om TRANSFIGURE
Les mer om GESTURE
Les mer om SCALP
Det er publisert en artikkel som oppsummerer all tilgjengelig sikkerhetsinformasjon fra både kliniske studier og bivirkningsovervåking på sekukinumab.
Les mer om den samlede sikkerhetsprofilen til sekukinumab her
Primære resultater fra de pivotale studiene (MEASURE 1 og 2) ved bruk av sekukinumab mot AS
- Baeten D, Sieper J, Braun J et al. Dominique et al. Secukinumab, an Interleukin-17A Inhibitor, in Ankylosing Spondylitis. N Engl J Med 2015;373:2534-2548.
- Deodhar AA, Dougados M, Baeten D et al. Effect of Secukinumab on Patient-Reported Outcomes in Patients With Active Ankylosing Spondylitis: A Phase III Randomized Trial (MEASURE 1). Arthritis Rheumatol. 2016 Dec;68(12):2901-2910.
Resultater fra studier med lengre varighet enn 1 år
- Marzo-Ortega H, Sieper J, Kivitz A et al. Secukinumab sustains improvement in signs and symptoms of patients with active ankylosing spondylitis through 2 years: Results from a phase 3 study [MEASURE 2]. Arthritis Care Res (Hoboken). 2017 Jul;69(7):1020-1029. doi: 10.1002/acr.23233. Epub 2017 Jun 7.
- Braun J, Baraliakos X, Deodhar A et al. Secukinumab shows sustained efficacy and low structural progression in ankylosing spondylitis: 4-year results from the MEASURE 1 study. Rheumatology (Oxford). 2019 May 1;58(5):859‐868. doi:10.1093/rheumatology/key375
- Baraliakos X, Braun J, Deodhar A, et al. Long-term efficacy and safety of secukinumab 150 mg in ankylosing spondylitis: 5-year results from the phase III MEASURE 1 extension study. RMD Open. 2019;5(2):e001005. Published 2019 Sep 3. doi:10.1136/rmdopen-2019-001005
Fem års effekt- og sikkerhetsdata fra den pivotale MEASURE 1-studien med Cosentyx mot ankyloserende spondylitt. Resultatene viste at effekten var opprettholdt over tid og sikkerhetsdatene viste at Cosentyx var godt tolerert med en sikkerhetsprofil i tråd med tidligere publikasjoner.
Sekukinumab som behandling etter TNFα-hemmer ved AS
Sammenfattende artikkel om IL-17A og patogenesen til AS samt resultater fra kliniske studier på sekukinumab
Sammenstilte sikkerhetsanalyser:
Utvikling av legemiddelantistoffer (immunogenitet):
Oversiktsartikler om IL-17:
Sekukinumab ble godkjent i 2015, og en rekke studier innenfor flere manifestasjoner av psoriasis er gjennomført etter dette.
En metaanalyse publisert i januar 2020 konkluderer med at sekukinumab viser solide resultater på effekt, drug survival og sikkerhet ved behandling av moderat til alvorlig plakk- psoriasis1. Analysen viser også en signifikant forbedring i DLQI ved behandling med sekukinumab1.

Effekt
Metaanalysen konkluderer med at 80% av pasientene oppnådde PASI 75 etter 12 måneders behandling.2 58% av pasientene hadde PASI 90 etter 12 måneders behandling. 51% av pasientene som fortsatte behandlingen med sekukinumab, og ble inkludert i analysen, oppnådde PASI 100 etter 12 måneder.1
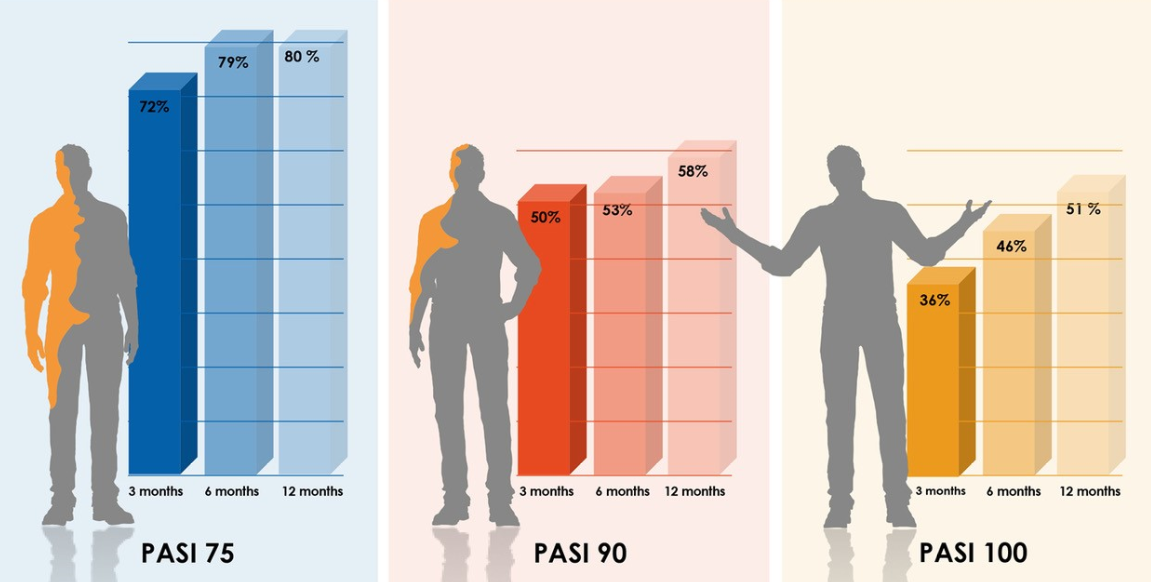
Figure adapted from Augustin et al. 2020. doi: 10.1111/JDV.16180

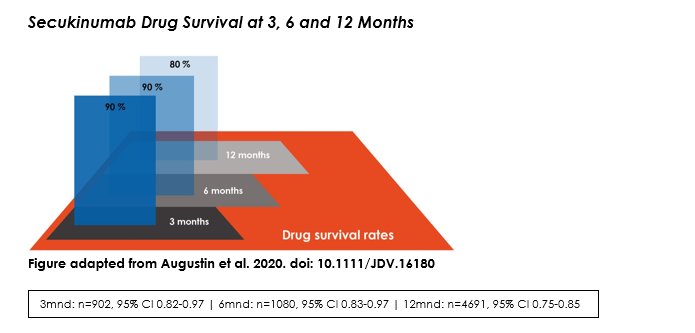
Drug survival
Drug survival gir viktig innsikt om langtidseffekt og sikkerhet for sekukinumab.
Data basert på 16.000 pasienter viser en drug survival på 90% etter 3 og 6 måneder.1 Etter 12 måneders behandling ser man en drug survival på 80%. Det er verdt å merke seg at sekukinumabs drug survival rate er sammenlignbar med ustekinumab (82%), og høyere enn 1 års survival rate for etanercept (66%) og adalimumab (69%).1
Etter 12 måneder er det bare 8% av pasientene som har sluttet med sekukinumab på grunn av tap av effekt.1