Her har vi samlet et utvalg av studier som vi håper du kan ha nytte av i din behandling av pasienter med alvorlig allergisk astma
Humbert M, Taillé C, Mala L et al; «Omalizumab effectiveness in patients with severe allergic asthma according to blood eosinophil count: the STELLAIR study” Eur Respir J. 2018 May 10;51(5)
Bousquet J, Brusselle G, Buhl R et al; “Care pathways for the selection of a biologic in severe asthma”, European Respiratory Journal 2017; 50: 170-178.
Humbert M, Beasley R, Ayres J et al; “Benefits of omalizumab as add-on therapy in patients with severe persistent asthma who are inadequately controlled despite best available therapy (GINA 2002 step 4 treatment): INNOVATE”, Allergy 2005;60:309-316.
Braunstahl G-J, Chen C-W, Maykut R et al; “The eXpeRience registry: The ‘real-world’ effectiveness of omalizumab in allergic asthma”, Respiratory Medicine 2013;107(8):1141-51.
Bousquet J, Siergiejko Z, Swiebocka E, et al; “Persistency of response to omalizumab therapy in severe allergic (IgE-mediated) asthma”, Allergy 2011 May:66:671-8
Korn S, Thielen A, Seyfried S et al; “Omalizumab in patients with severe persistent allergic asthma in a real-life setting in Germany”, Resp Med 2009;103:1725–31
Braunstahl G-J, Canvin J, Peachey G et al; “Healthcare Resource Utilization in Patients Receiving Omalizumab for Allergic Asthma in a Real-World Setting”, Biol Ther 2014; 4:57-67
POLYP-1 og POLYP-2 er to fase III-studier, gjennomført for å evaluere effekten og sikkerheten til omalizumab, versus placebo hos voksne pasienter, med kronisk rhinosinusitt med nasal polypose (CRSwNP) med utilstrekkelig respons på standard behandling, intranasale cortikosteroider (INC)
Sammendrag
Kronisk rhinosinusitt med nasal polypose (CRSwNP) er karakterisert ved IgE overproduksjon og eosinofil inflammasjon. IgE antas å spille en sentral rolle ved kronisk rhinosinusitt med nesepolypper (CRSwNP) patogenese ved å aktivere inflammatoriske celler av type 2 som mastceller, basofile og eosinofile granylocytter.
POLYP-1 og POLYP-2 er to replikate fase III-studier designet for å undersøke effekten og sikkerheten til omalizumab ved kronisk rhinosinusitt med nasal polypose (CRSwNP), hos pasienter som har utilstrekkelig respons på standard behandling, intranasale kortikosteroider (INC).
Begge studiene var randomiserte, multisenter, dobbeltblinde og placebokontrollerte. Pasienter i studiene ble randomisert (1:1) til omalizumab eller placebo i 24 uker, gitt ved subkutan injeksjon hver andre til fjerde uke.
Alle pasienter fikk i tillegg intranasal mometason i disse 24 ukene.
Begge studiene møtte begge de primære endepunktene:
endring fra baseline til uke 24 i Nasal Polyp Score (NPS) og Nasal Congestion Score (NCS) for omalizumab versus placebo. Resultatene var som følger:
NPS: –1,08 versus 0,06 (P <0,0001) og –0,90 versus –0,31 (P = 0,0140)
NCS: –0,89 versus –0,35 (P = 0,0004) og –0,70 versus –0,20 (P = 0,0017)
Sekundære endepunkter
Sino-Nasal Outcome Test-22 (SNOT-22), University of Pennsylvania Smell Identification Test (UPSIT), luktesans, postnasal drypp og rennende nese forbedret seg også betydelig med omalizumab kontra placebo med intranasal mometason som grunnmedisinering.
Forekomst av bivirkninger var balanserte mellom gruppene. Ingen nye eller uventede sikkerhetsproblemer ble identifisert med omalizumab.
Oppsummert forbedret omalizumab signifikant endoskopiske, kliniske og pasientrapporterte resultater hos pasienter med CRSwNP som var refraktær mot intranasale kortikosteroider, og ble godt tolerert.
Studiesentre

Studiedesign
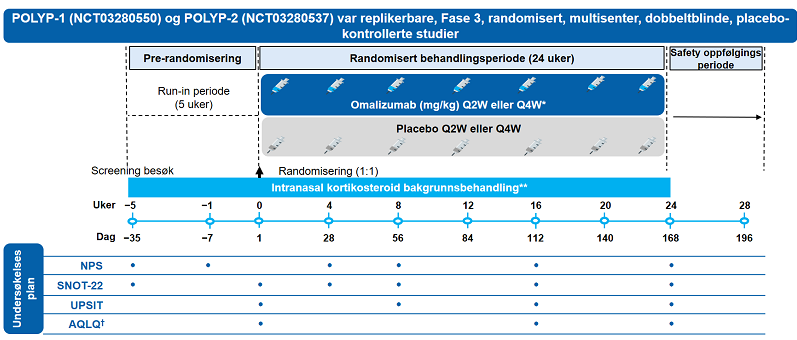
Saltskylling i nesen var tillatt under studien. Men fordi antibiotika ofte brukes til å behandle CRSwNP, var systemisk antibiotikabehandling i> 14 dager ikke tillatt i løpet av studien.
* Dosen av omalizumab ble bestemt basert på total s-IgE nivåer og kroppsvekt ** Alle pasienter fikk intranasale kortikosteroider (mometason nesespray) som bakgrunnsbehandling † AQLQ ble sendt ut til pasienter med komorbid astma, AQLQ = Asthma Quality of Life Questionnaire, spørreskjema om astmakvalitet; NPS = nasal polypp score; Q2W = annenhver uke; Q4W = hver 4. uke; SNOT-22 = sino-nasal output test-22; UPSIT = University of Pennsylvania luktidentifikasjonstest
Inklusjons- og eksklusjonskriterier

IgE = immunoglobulin E; INCS = intranasale corticosteroids; NCS = nasal congestion score; NPS = nasal polyp score; SCS = systemic corticosteroids; SNOT-22 = sino-nasal outcome test-22
Primære og sekundære endepunkt
De primære endepunktene for begge studiene var endring fra baseline til uke 24 i Nasal Polyp Score (NPS) og Nasal Congestion Score (NCS) for omalizumab sammenlignet med placebo.
Sekundære endepunkter inkluderte endring fra baseline til uke 24 i Sino-Nasal Outcome Test-22 (SNOT-22) score, University of Pennsylvania Smell Identification Test, luktesans, postnasal drypp, rennende nese og bivirkninger.
Resultater
Pasientfordeling
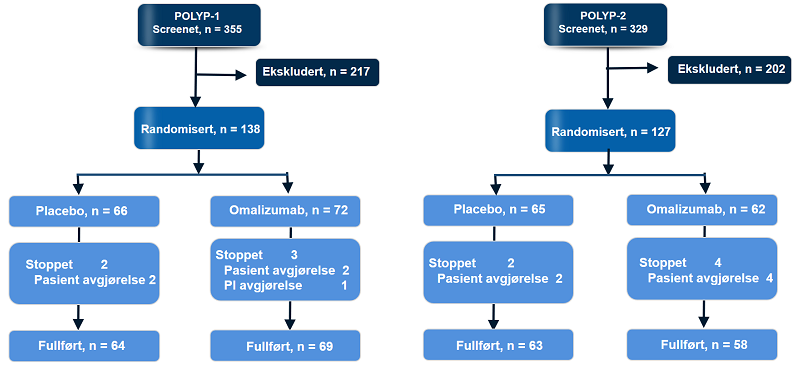
PI= principal investigator
Pasienter i POLYP 1 (n = 138) og POLYP 2 (n = 127) hadde alvorlig CRSwNP og betydelig livskvalitetsnedsettelse, vist med en gjennomsnittlig NPS høyere enn 6 og SNOT-22-score på omtrent 60.
Begge studiene møtte begge de primære endepunktene, endring fra baseline til uke 24 i Nasal Polyp Score (NPS) og Nasal Congestion Score (NCS) for omalizumab sammenlignet med placebo;
Koprimære endepunkter: Omalizumab reduserte signifikant NCS og NPS versus placebo ved uke 24
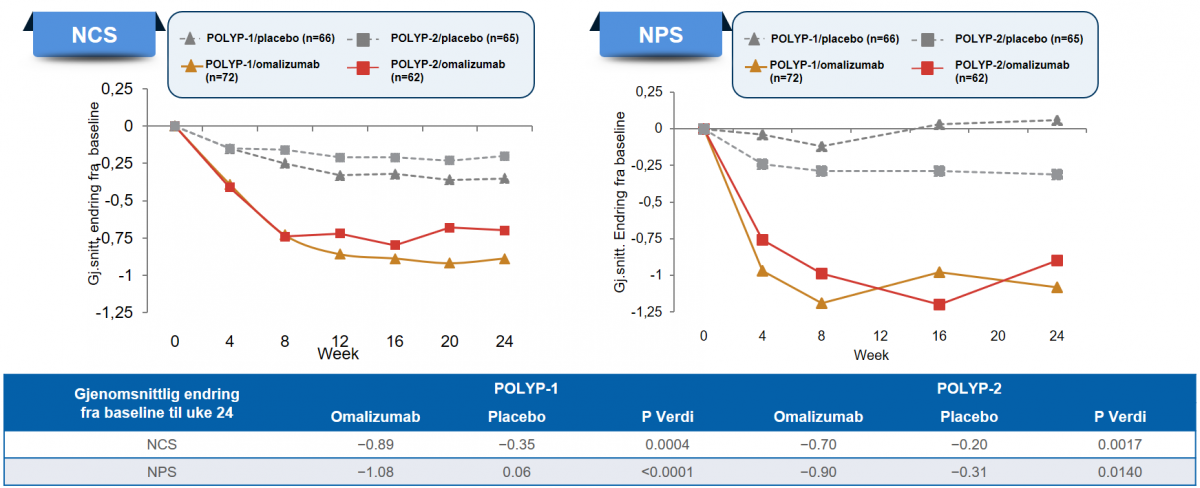
Placebokontrollerte forbedringer i NCS og NPS ble observert i uke 4 i begge studier (p<0.05, ikke justert for mangfold)
NCS = nasal congestion score; NPS = nasal polyp score
- NPS: –1,08 sammenlignet med/versus 0,06 (P <0,0001) og –0,90 sammenlignet med/versus –0,31 (P = 0,0140)
- NCS: –0,89 sammenlignet med –0,35 (P = 0,0004) og –0,70 sammenlignet med/versus –0,20 (P = 0,0017)
Sekundære endepunkt: Omalizumab forbedret QoL (Quality of Life), luktesans, og nesesymptomer versus placebo over 24 uker
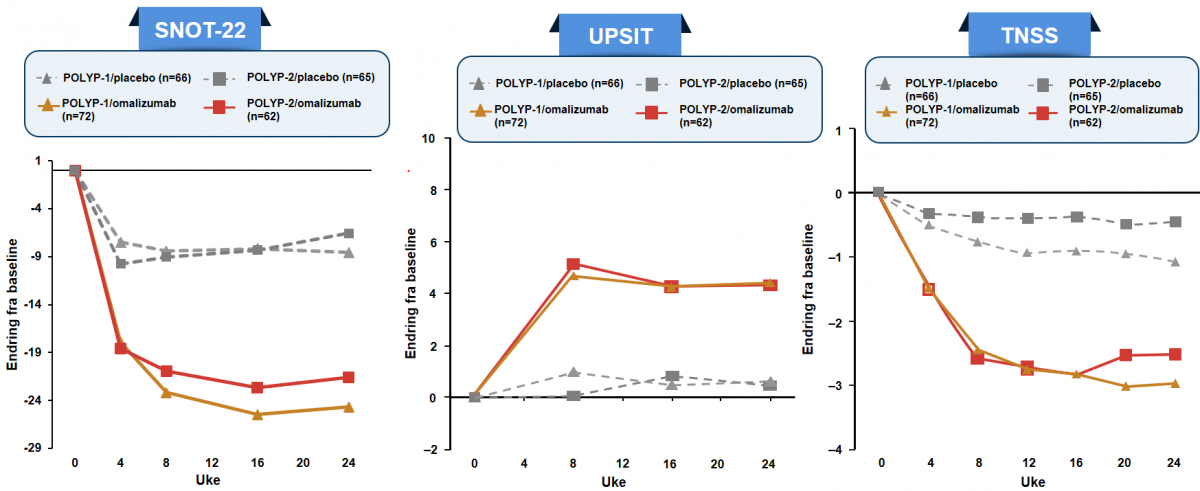
SNOT-22 MCID: 8.9
LSM = least squares mean; SNOT-22 = sino-nasal outcome test-22; TNSS =total nasal symptom score; UPSIT = University of Pennsylvania smell identification test
- SNOT-22-score, –24,7 versus –8,6 (P <.0001) og –21,6 versus –6,6 (P <0,0001)
Sikkerhet
Det var ingen forskjell i bivirkninger mellom gruppene. Omalizumab ble godt tolerert. Det var heller ingen nye eller uventede bivirkninger som ble observert med omalizumab.. De vanligste bivirkninger var hodepine, reaksjon på injeksjonssted, atralgi, svimmelhet, øvre abdominalsmerte. Disse bivirkningene er tilsvarende som for omalizumabs øvrige godkjente indikasjoner, allergisk astma og spontan kronisk urtikaria.
Konklusjon
Oppsummert, så viste omalizumab en signifikant bedring av endoskopiske, kliniske og pasientrapporterte
resultater hos pasienter med kronisk rhinosinusitt og nasal polypose, som ikke responderte på behandling med intranasale kortikosteroider.
- I POLYP-1 og POLYP-2 viste omalizumab statistisk signifikante forbedringer i de koprimære endepunktene, NPS og gjennomsnittlig daglig NCS, sammenlignet med placebo i uke 24 mens de fikk intranasalt mometason som grunnmedisinering.
- Omalizumab resulterte også i signifikante forbedringer i pasientrapporterte vurderinger av alvorlighetsgraden av symptomer versus placebo
- Forbedringer i SNOT-22 indikerer innvirkning på pasientens livskvalitet og plasserer resultatene i viktig sammenheng i forhold til andre behandlinger som SCS og kirurgi
- Omalizumab ble godt tolerert, og bivirkninger var i samsvar med de tidligere rapporterte
- Omalizumab representerer et lovende nytt behandlingsalternativ for pasienter med refraktær CRSwNP
Referanse
-
Gevaert P, Omachi TA, Corren J et al. J Allergy Clin Immunol 2020. doi: https://doi.org/10.1016/j.jaci.2020.05.032

